
Porque é difícil uma vacina este ano
Há três fases para que uma vacina seja liberada, no Brasil o 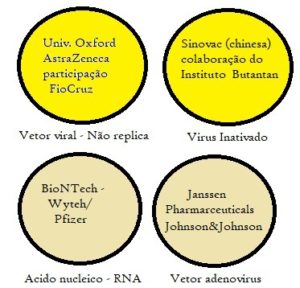 órgão responsável pela avaliação e aprovação de solicitações para realização de pesquisas clínicas com fins de registro e de pedidos de registro de produtos imunobiológicos desenvolvidos na indústria farmacêutica é feito pela Anvisa (Agência Nacional de Vigilância Sanitária), há comitês de ética que acompanham as etapas dos estudos, os Comitês de Ética em Pesquisa (CEPs) e/ou da Comissão Nacional de Ética em Pesquisa (CONEP), então há critérios e cuidados que são observados.
órgão responsável pela avaliação e aprovação de solicitações para realização de pesquisas clínicas com fins de registro e de pedidos de registro de produtos imunobiológicos desenvolvidos na indústria farmacêutica é feito pela Anvisa (Agência Nacional de Vigilância Sanitária), há comitês de ética que acompanham as etapas dos estudos, os Comitês de Ética em Pesquisa (CEPs) e/ou da Comissão Nacional de Ética em Pesquisa (CONEP), então há critérios e cuidados que são observados.
Na fase 1, são selecionados pequenos grupos de voluntários, normalmente adultos saudáveis, são avaliados para a verificação da segurança e determinação do tipo de resposta imune provocada pela vacina, na fase 2, há a inclusão de um maior número de indivíduos e o produto é administrado em indivíduos representativos da população com menores proteções imunológicas (crianças, adolescentes, idosos e pessoas com imunologia comprometida), já na terceira fase é preciso aplicar numa grande quantidade de indivíduos e garantir o mínimo possível de reações adversas e contra-indicações, nesta etapa o número de voluntários deve ser grande.
A empresa só vai solicitar o registro de produtos com estudos na fase 3 em andamento, assim os dados das etapas 1 e 2 devem estar consolidados e sua eficiência demonstrada com alta eficiência terapêutica e/ou preventiva, e não exista terapia alternativa comparável aquele estágio da doença, aqui entra em cena o jogo dos interesses econômicos que podem ser levados para o campo político e até mesmo de disputa de mercados, porém é de se esperar que no caso da Covid-19 haja alguma ética neste processo.
Há 26 vacinas em estágio avançado, mas as quatro vacinas com potencial uso no Brasil são de quatro técnicas diferentes: o vetor viral é a técnica de Oxford e AstraZeneca que tem colaboração da FioCruz brasileira, a do laboratório chinês Sinovac tem participação do Instituto Butantan, a BioNTech – Wytech/Pfizer tem laboratórios privados no Brasil e anunciou que poderia estar pronta em Outubro, e, a Janssen Pharmaceuticals (Johnson & Johnson) adota a técnica do vetor de adenovírus (veja as técnicas e colaborações na figura).
A Sinovac com a técnica de vírus inativado poderá estar pronta para o ano que vem, a Janssen não fez grandes anúncios ainda, mas sabe-se que irá para a terceira fase, e a mais promissora que é a de Oxford está na fase 3, mas não deverá estar disponível até na melhor das hipóteses em dezembro.
De acordo com a Anvisa, o prazo para a manifestação sobre a vacina é de até 60 dias, embora a Anvisa tenha acelerado o processo de pedidos para medicamentos e vacinas no caso da Covid-19 instituiu um Comitê de Avaliação de Estudos Clínicos, Registro e pós-registro de Medicamentos, que inclui vacinas.
Assim ainda que o pedido esteja encaminhado em Outubro o provável de sua aprovação é para dezembro, até iniciar a produção e colocar a disposição dos órgãos de saúde deverão estar pronta para início da vacinação em meados de janeiro, antes disto cuidado, prevenção e manter as esperanças.
Enquanto isto estamos, no Brasil, paralisados num patamar de mil mortes diárias.









